研究内容
汚染水を浄化するための固体触媒の開発
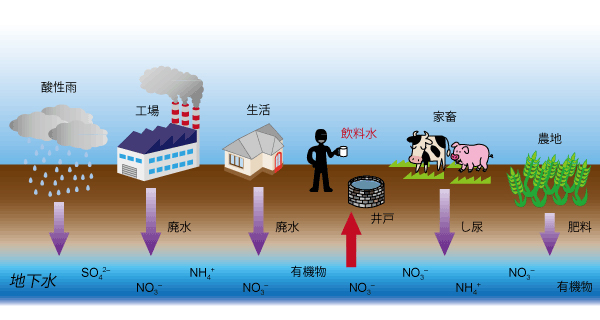
私たちは外国から多くの農作物や畜産酪農製品、工業製品を輸入しているので、それらの国々の水を間接的に消費しています。 世界の国々において社会が持続的に発展するためには、清浄な飲料水を長期にわたって確保することが不可欠です。 しかし、近年、様々な人的要因によって生活圏の地下水汚染が深刻になってきました。
私たちは地下水や廃水中のNO3–やNH4+を、無害なN2へと変換する固体触媒を研究しています。
担持パラジウム合金触媒による水中硝酸イオンの接触水素化分解
農地への過剰な施肥、畜産廃棄物の不適切な処理、生活排水の混入を原因とする地下水のNO3–汚染が問題になっています。 NO3–に汚染された水を飲み続けると、メトヘモグロビン血症や糖尿病、高血圧などを発症すると指摘されています。 乳幼児は特に危険で、死に至ることもあります。NO3–を無害なN2へと変換し、汚染水から取り除かなればなりません。 現在、いくつかの浄化法が提案されています。例えば、生物学的方法(微生物による分解)やイオン交換法があります。 しかし、これらは高コスト、煩雑な操作が必要、二次汚染水の発生等、問題があります。 これらの問題を回避する手法として、固体触媒を使ってNO3–をH2と反応(接触水素化)させN2へと変換する方法が注目されています。
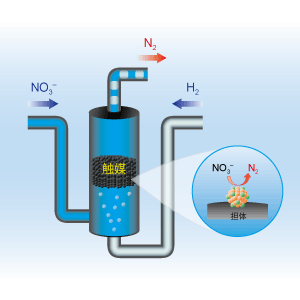
目的とする反応
2NO3– + 5H2 → N2 + 2OH– + 4H2O
望ましくない副反応
NO3– + 4H2 → NH3 + OH– + 2H2O
私たちは、大気圧下、室温付近といった穏和な条件で水中のNO3–をN2へとほぼ100%変換する活性炭担持Cu-Pd合金クラスター触媒を開発しました。 実際の地下水には、NO3–以外に様々なイオンや水溶性有機化合物が含まれており、これらは触媒に悪影響を与えます。私たちは、地下水をあらかじめオゾン酸化処理することで、実際のNO3–汚染地下水を浄化できることを実証しました。 また、水中にNO3–以外のイオンが存在しても触媒特性が変化しない、活性炭担持Sn-Pd合金触媒を見いだしています。
担持ニッケル触媒を用いた水中硝酸イオンの接触水素化分解
Cu-Pd合金やSn-Pd合金などの担持パラジウム合金触媒は、水中NO3–をN2へと効率的に変換します。 しかし、Pdは資源量も限られており、かつ高価な貴金属です。 そのため、資源量が豊富で安価な金属からなる高性能な触媒が強く求められています。 私たちは、Pdに比べて極めて安価なNiに注目しました。 活性炭担持Pd合金触媒と同様、活性炭担持Ni触媒も温和な条件下での水中NO3–水素化分解に活性を示しました。 しかし活性炭担持Ni触媒は、N2への選択率が低いことが問題です。 私たちは、この問題を解決すべく研究を進めています。
光触媒反応による水中硝酸イオンの光還元分解
これまで説明して来ました担持金属触媒による水中NO3–水素化分解では、水素ガスをNO3–の還元剤に使います。 しかし、一般にはH2ガスの取り扱いは難しく、また何処でも手軽に入手できるものではありません。 H2ガスを用いない浄化法として光触媒反応に注目しました。
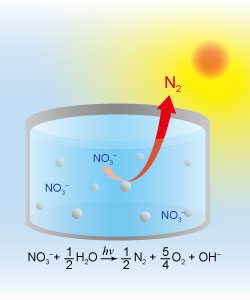
私たちは、光触媒反応によってその場で(水中で)H2を発生させ、担持金属触媒上で発生させたH2とNO3–を反応させることを考えました。 犠牲試薬存在下、紫外光を駆動力としてH2を発生するPt/TiO2とSn-Pd/Al2O3の両方をNO3–水溶液に分散させ、エタノール存在下で紫外光を照射したところ、NO3–はN2へと変換されました。 私たちの光触媒系は、異なる反応を促進する触媒を独立に設計・開発できるので触媒設計の自由度が高く、より高性能な光触媒系を開発できる可能性を秘めていると考えています。 可視光を駆動力とした水中NO3–光還元分解やH2Oを還元剤した水中NO3–光還元分解を効率的に促進する光触媒系を開発する事が私たちの目標です。
水中アンモニウムイオンの接触オゾン酸化分解
アンモニアは湖沼水や閉鎖海域の富栄養化を起こす原因物質なので、工場廃水や生活排水に含まれるアンモニアは除去されなければなりません。 担持貴金属触媒を使った酸素ガスを酸化剤とした水中アンモニアの酸化分解が報告されていますが、150℃以上の高温でなければ反応が進行せず問題となっていました。 私たちは、酸素ガスよりも酸化力の強いオゾン(O3)を酸化剤とした、水中アンモニアの酸化分解に取り組んでいます。
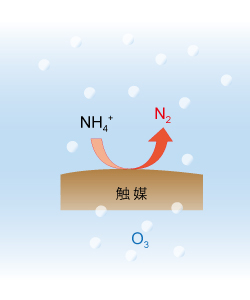
目的とする反応
6NH4+ + 9O3 → 3N2 + 6H+ + 9H2O + 9O2
望ましくない副反応
NH4+ + 4O3 → NO3– + 2H+ + H2O + 4O2
これまでに、反応中の溶解がほとんど無く、かつマイルドな温度でも高い触媒活性を示しN2選択性も高い酸化コバルト触媒を見いだしています。 触媒活性の更なる向上と望ましく無いNO3–の生成を完全に抑制すべく研究を進めています。
ヘテロポリ酸を用いた固体触媒の開発
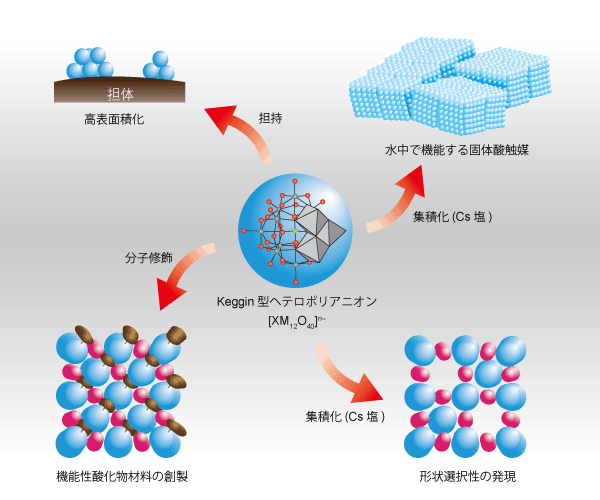
Keggin型ヘテロポリ酸は、強いブレンステッド酸点を持ち、熱的・化学的にも安定な酸化物クラスターです。 ヘテロポリ酸の特徴は、その分子性です。通常の固体酸化物では原子を最小単位としてその構造を考えますが、固体のヘテロポリ化合物ではヘテロポリアニオン※が基本ユニットです。 ヘテロポリアニオンの構成元素の一部を取り除いたり、さらにそこに官能基や触媒活性点となる原子団を比較的容易に導入する事ができます。 このように分子設計されたヘテロポリアニオン(もしくはヘテロポリ酸)を規則的に集積化することで、触媒をはじめ様々な機能性固体材料が合目的に合成できると考えています。
※ヘテロポリ酸を構成しているアニオンのこと。対カチオンがH+のヘテロポリ化合物をヘテロポリ酸と呼ぶ。
分散化ヘテロポリ固体酸触媒
Keggin型ヘテロポリ酸(H3[PW12O40]、H4[SiW12O40])は、強いブレンステッド酸点を持つため、固体酸触媒として機能します。 しかし、表面積が小さい(約5 m2 g-1)ので、実際に使える触媒にするには表面積を拡大しなければなりません。 私たちは、Keggin型ヘテロポリ酸の表面積を大きくするために、ヘテロポリ酸を高表面積な酸化物担体上に分散化させました。 この分散化ヘテロポリ酸触媒は、Friedel-Crafts反応、アルカン骨格異性化、二重結合異性化、エチレン水和などの酸触媒反応に高い活性を示しました。 また、分散化ヘテロポリ酸触媒に微量のアルカリ金属イオンを添加すると酸強度が弱くなり、これによってiso-ブテンの優先的オリゴマー化(iso-ブテン/n-ブテン混合物中のiso-ブテンを優先的にオリゴマー化する)を高選択的に進行させることができるようになりました。
従来、担体上への分散化は、表面に露出するヘテロポリ酸の数を増やすことにのみ寄与していると考えられていました。 最近、私たちはSiO2の表面に分散化されたH4[SiW12O40]は、H4[SiW12O40]が元来、備えていたブレンステッド酸よりも強い酸性を発現することを見いだしました。 すなわち、担体との相互作用によってヘテロポリ酸の質的変化が誘因されたと言う事です。 現在、発現メカニズムの解明や更に強いブレンステッド酸点を発現させる方法論を探索しています。
特異な触媒特性および分子吸着特性を示す集積化ヘテロポリ化合物
4価のKeggin型ヘテロポリアニオン([SiW12O40]4-)をセシウムカチオン(Cs+)と反応させて合成したセシウム塩は、規則的なマイクロ孔を持つ多孔性固体である事を見いだしました。 一部の対カチオンをH+として残したCs3H[SiW12O40]が、分子サイズによって反応基質を見分ける、分子サイズ選択的な固体酸触媒となります。 このセシウム塩をエタノール中で加熱処理すると、マイクロ孔は維持されたままメソ孔が新たに形成されます。 このバイモダルな細孔を持つセシウム塩触媒は、比較的に大きな分子サイズの反応基質に対して有効に機能することが期待されます。
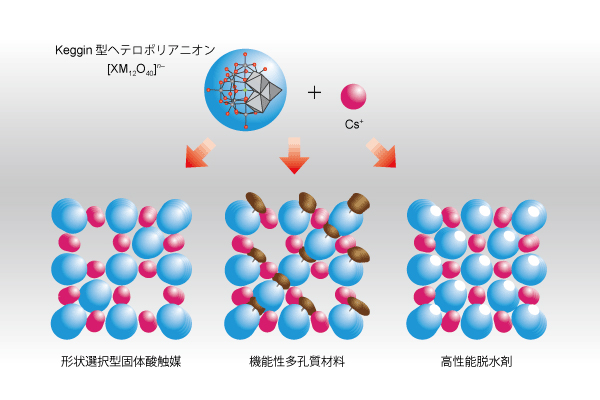
一方、有機基を導入した4価のKeggin型ヘテロポリアニオンのセシウム塩は、導入した有機基によってユニークな分子吸着特性を示すマイクロ多孔体となります。 例えば、アルキル基を導入したセシウム塩は疎水的な吸着特性を示します。また、細孔サイズに近いフェニル基を導入したセシウム塩は、温度によって吸着特性がダイナミックに変化するようになります。
構成元素の一部を取り除いた一欠損Keggin型ヘテロポリアニオンのセシウム塩は、水やメタノールなどの極性が高くかつサイズの小さい基質のみを、その結晶内部に取り込む特異な分子収着特性を示します。 この特性を利用すると、エタノールに含まれる微量な水分を除去することができます。バイオエタノール中の微量水分除去への応用が期待されます。
炭化水素化合物を高選択に酸化する固体触媒
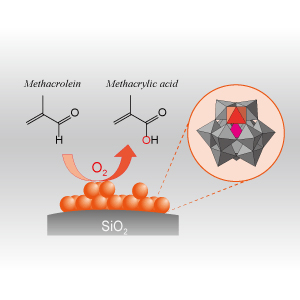
P-Mo-Vを構成元素としたKeggin型ヘテロポリ酸(H4[PMo11VO40])は、メタクロレインを酸化してメタクリル酸にする固体触媒です。 H4[PMo11VO40]をSiO2担体上に分散化すると、触媒活性が向上します。しかし、メタクリル酸への選択率は低下してしまいます。 高温のアンモニア雰囲気下で処理したSiO2を担体に用いる事で、分散化に伴うメタクリル酸選択率の低下を抑制する事ができました。 担体上でのアンモニウム塩の形成が、選択率向上の理由です。 ヘテロポリ酸触媒上でメタクロレインは、どのように酸化されているのか?に答えるため研究を進めています。
リン資源回収のための固体触媒の開発
廃水からのリン酸の回収
リン酸肥料の原料であるリン鉱石の枯渇が懸念されています。 リン鉱石が枯渇すれば、近代的な農業は全く行う事ができません。 石油などの化石資源と異なり、リンを代替するもの(元素)はありませんので、使用したリンをどこかで回収するしかありません。 私たちは、触媒反応によって廃水中のリン酸イオンを選択的に回収し、再利用できる技術を開発するための研究を開始しました。 近いうちに良い結果を報告できるよう、頑張っています。
温室効果ガスの無害化,資源化のための触媒開発
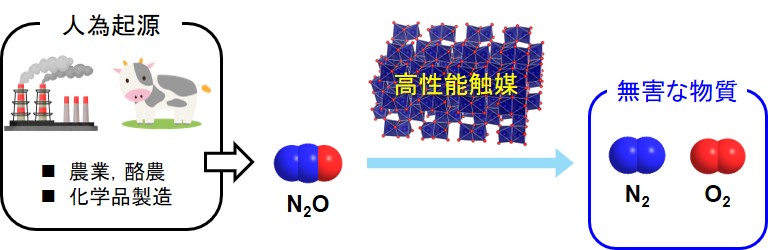
CO2に代表される温室効果ガスは地球温暖化の原因物質であり、気候変動など私たちの生活に関わるさまざまな問題を引き起こします。亜酸化窒素N2OやメタンCH4はCO2より高い温暖化係数をもつ温室効果ガスであり,農業、酪農、製造業などの人為起源で発生します。
私たちはこれらの温室効果ガスを無害化または資源化するための高性能触媒の開発を行っています。
(この研究は、JKA補助事業の支援を受けて実施しました)