研究広報
硝酸イオン汚染地下水を完全に浄化できる2段法プロセスの開発
要 約
新しい固体触媒プロセスが開発された。このプロセスは2種類の触媒から構成される。2種類の触媒が、水素ガスによって、ほぼ完全に水中の硝酸イオン(NO3-)を浄化した。しかも、このプロセスは、従来の処理法より、低コストで小規模に浄化できそうだ。プロセスの低コスト、小規模化は、触媒性能の向上によって実現できる。今後、触媒性能をさらに高め、一般家庭への導入を目指す。
近年、NO3-汚染水を浄化する技術の確立が、急務となっている。
それは、NO3-が身近な有害物質になったからである。すなわち、NO3-は飲料水に含まれている。飲料水は主に地下水から供給されている。この地下水が、最近、NO3-によって汚染されてきているのだ。NO3-に汚染された水を飲み続ける事は、生命にとって危険な行為である。例えば、メトヘモグロビン血症(注1)や糖尿病、高血圧などが発症すると指摘されている。このような病気を防ぐためには、汚染水中のNO3-を99%以上の割合で(注2)、無害な物質に分解する必要がある。具体的には、窒素(N2)への還元である。そのための浄化法が、いくつか考案されている。しかし、まだ確立には至っていない。例えば、生物化学的な方法やイオン交換法がある。いずれも高コストである事が、問題になっている。
今回、NO3-を無害化する新しいプロセスが考案された。
それが、表題の2段触媒プロセスである。このプロセスは、2つの触媒を活用している。1つめの触媒は、活性炭(AC)に担持したCu-Pdクラスター触媒である。この触媒をCu-Pdクラスター/ACと表記する。Cu-Pdクラスター/ACは、NO3-を高選択的に亜硝酸イオン(NO2-)へ還元する。2つめの触媒は、βゼオライトに担持したPd触媒である。この触媒をPd/βゼオライトと表記する。Pd/βゼオライトは、NO2-をN2とN2O(注3)へ効率的に分解する。これらの触媒を組み合わせる事で、NO3-をN2とN2Oに還元できる。
この新しいプロセスの特徴は、2つの触媒を利用している点にある。
従来のプロセスは、1つの触媒でNO3-を直接N2へ還元していた。そのような触媒として、Cu-Pd触媒が有効であると報告されていた。従来のプロセスの問題点は、N2の他に、アンモニア(NH3)が生成する事である(Fig. 1)。アンモニアは飲料水に悪臭をもたらす。そのため、水中のアンモニア濃度を0.5 ppm以下に抑える必要がある。新しいプロセスでは、NO3-を2つの触媒で段階的に還元する。これによって、アンモニア生成の抑制を達成した。
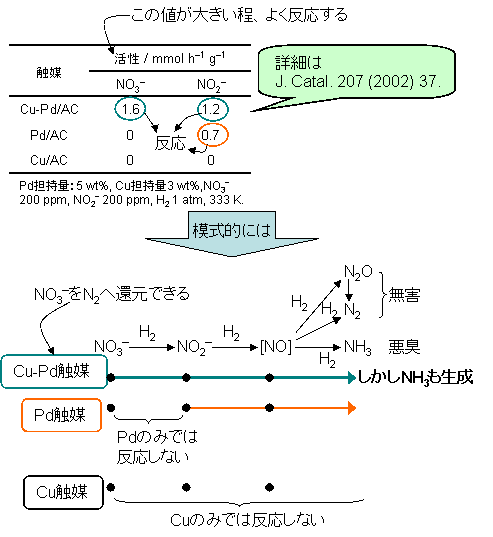
Fig. 1 これまでの触媒プロセスとアンモニアの生成
まず、Cu-Pdクラスター/ACが、NO3-を高選択的にNO2-へ還元する。
これは特異な現象である。なぜならば、上記の通り、Cu-Pd触媒は、NO3-をN2に還元する触媒として報告されているからだ。しかし、Cu-Pdをナノスケールのクラスターに細分化すると、NO3-がNO2-へ選択的に還元される事が分かった(Fig. 2)。なお、この反応のpH(水素イオン濃度)制御は、不要である(注4)。これは低コスト化を期待させる。

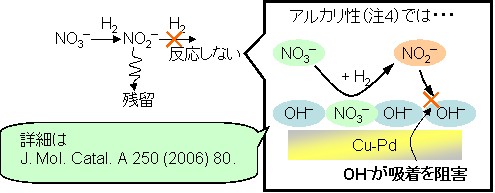
Fig. 2 Cu-Pdクラスター/ACとNO3-からNO2-への選択還元
次に、Pd/βゼオライトが、NO2-をN2とN2Oへ還元する。
この反応は、中性条件(pH = 7)で行う。このような条件では、NH3を全く発生させない事が分かった(Fig. 3)。なお、中性条件は、二酸化炭素を使うだけで、簡単に達成できる。

Fig. 3 アンモニアがほとんど生成しないNO2-還元
これらの触媒を組み合わせる事で、NO3-をほぼ完全に浄化できた。
この2段触媒プロセスは、Fig. 4のように2つのリアクターから構成される。1つめが、Cu-Pdクラスター/ACを触媒とする1段目リアクターである。2つめが、Pd/βゼオライトを触媒とする2段目リアクターである。各リアクターでNO3-汚染水が順次、処理される。この処理で生成したアンモニアの濃度は、0.6 ppmであった(Fig. 4)。この濃度は、水質的な目標値である0.5 ppm以下に迫る値である。
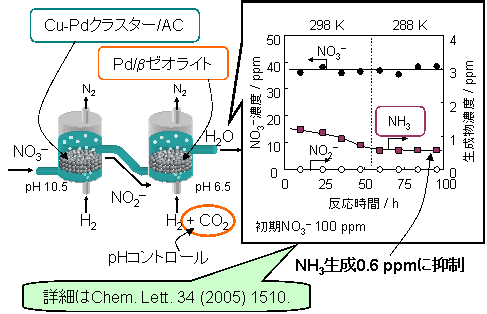
Fig. 4 2段触媒プロセスによるNO3-還元
これにより、各家庭においてNO3-汚染水を処理できる日も近くなった。
それは触媒法が、家庭で処理するための条件を備えているからだ。家庭で処理するために満たすべき条件は、少なくとも2つある。1つは、処理装置が小型な事である。もう1つは、処理費が安価な事である。これら2つの条件をバイオ法などの他の処理法は、満たしていなかった。しかし、触媒法では、これらの2つの条件を満たせるであろう。触媒法で条件を満たす方法は、以下の2つである。
- 水素ガスを安価に供給し、処理費を安くする。
これは、水の電気分解装置を用いる事で解決できる。水の電気分解装置なら、家庭の電源を使って、安く水素ガスを得る事ができる。また、充分な量の水素ガスを小型な装置で供給できる。これは触媒法の小型化に貢献する。これとは別に、必要な水素ガス量を少なくする事で、処理費を安くする事もできる。そのためには、触媒が無駄なく水素ガスを利用する必要がある。これは、触媒と水素ガスを接しやすくする事で達成できる。具体的には、触媒表面を疎水的にする。
- 触媒性能の向上で、処理装置を小型化する。
1 gの触媒が1時間あたりに処理できるNO3-の量を触媒活性と呼ぶ。触媒活性を上げれば、より少ない触媒で、NO3-汚染水を処理できる。触媒量が減れば、装置をさらに小型にできる。触媒活性の向上は、ナノサイズの金属粒子やナノサイズの担体を用いる事で可能になるだろう。
これらを今後検討する事で、小規模かつ安価に、NO3-汚染水を処理できるであろう。
脚 注
- 注1)「メトヘモグロビン血症」
-
体内の酸素供給が不十分になり、チアノーゼ症状を引き起こす事。酸素を供給する赤血球が、機能しなくなる病気である。赤血球には、酸素を格納するための分子が存在する。この分子を「ヘモグロビン」と呼ぶ。そして、酸素を格納する機能を失ったヘモグロビンが「メトヘモグロビン」である。ヘモグロビンの10%がメトヘモグロビンになると、体内で酸欠が起こる。
NO3-によってメトヘモグロビン血症が引き起こされる。そのメカニズムは、次の通りである。NO3-が飲料水に混入する。飲料水が胃に到達する。胃にはNO3-をNO2-に還元する細菌がいる。この細菌がNO3-を一部NO2-に変える。NO2-は腸で吸収され、血液に入る。血液中のヘモグロビンがNO2-と反応して、メトヘモグロビンになる。メトヘモグロビンの割合が10%を超えると、発症。
この症状は、乳幼児で起こりやすい。乳幼児の胃では、NO3-がNO2-になりやすいためである。この反応は、胃の中のpHが高いと起こりやすい。乳幼児の胃では、胃酸の分泌が少ないため、pHが高くなっている。大人は胃酸の分泌が多いので、pHは低い。そのため、大人では、ほとんど発症しない。
- 注2)「NO3-を99%以上の割合で」
-
飲料水にするためには、NO3-を50 ppm以下、NO2-を3 ppm以下にする必要がある。世界保健機構(WHO)のガイドライン1998年版より。
- 注3)「N2O(亜酸化窒素)」
-
低濃度なら無害。しかし、温室効果を有する。実験では、以下の方法で、N2OをすべてN2に還元できた。プロセスの気体出口に、Pd/ACを接続する。Pd/ACが水素ガスによってN2OをN2へ還元した。
- 注4)「pH制御は、不要」
-
液がアルカリ性になる。NO3-のマイナスが、OH-に保存されるため。
2NO3- + 5H2 → N2 + 2OH- + 4H2O
なお、このOH-は、NO2-還元を阻害する(Fig. 2)。NO2-還元が阻害されるため、NO3-還元で、NO2-が、選択的に生成する。
参考論文
- 【Cu-Pdクラスター触媒関連】
-
Cu-Pd bimetallic cluster/AC as a novel catalyst for the reduction of nitrate to nitrite, Yoshinori Sakamoto, Kou Nakata, Yuichi Kamiya, and Toshio Okuhara, Chem. Lett. 33 (2004) 908.
Selective Hydrogenation of Nitrate to Nitrite in Water over Cu-Pd Bimetallic Clusters Supported on Active Carbon, Yoshinori Sakamoto, Yuichi Kamiya and Toshio Okuhara, J. Mol. Catal. A 250 (2006) 80.
- 【2段触媒プロセス関連】
-
A Two-Stage Catalytic Process with Cu-Pd Cluster/Active Carbon and Pd/β-Zeolite for Purification of Water by Nitrate Hydrogenation, Yoshinori Sakamoto, Kyosuke Nakamura, Rie Kushibiki, Yuichi Kamiya, and Toshio Okuhara, Chem. Lett. 34 (2005) 1510.